Curiethérapie de la prostate
Une destruction efficace de cellules cancéreuses
On observe depuis les années 2000, en particulier aux États-Unis et en Europe, un recours accru à la curiethérapie pour les traitements des cancers de la prostate. La curiethérapie de la prostate consiste à installer dans cette glande des implants radioactifs constitués d’une source radioactive enrobée dans une capsule de titane. Deux radioéléments artificiels sont utilisés, l’iode-125 et le palladium-103.
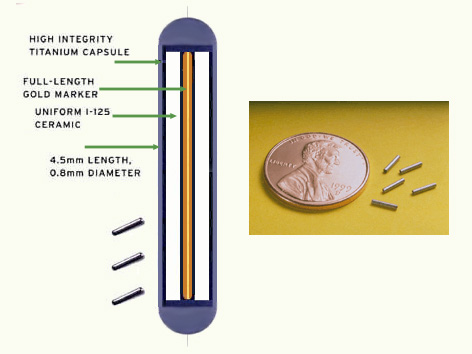
Implants pour les cancers de la prostate
La taille d’un implant est celle d’un grain de riz. Les deux radioéléments artificiels introduits dans ces implants, l’iode-125 (I-125) et le palladium-103 (Pd-103), émettent des électrons d’énergie relativement faible. Les électrons ne sont pas assez énergiques pour sortir des implants. L’irradiation est due aux rayons X qui sont principalement absorbés dans les tissus cibles entourant l’implant.
© Kimmel Cancer Center at Jefferson.
Pourquoi ces deux radioéléments ? Ils ont en commun de se désintégrer par capture électronique, un mode de désintégration rare qui dépose peu d’énergie dans le milieu (Celle-ci est majoritairement emportée par un neutrino, une particule qui ne laisse aucune trace dans le corps du patient !). Des électrons (électrons de conversion, électrons Auger et des rayons X sont toutefois émis au cours du réarrangement de l’atome qui suit la capture.
Les électrons, dont l’énergie est plus faible que celle des électrons bêta normaux, sont absorbés par les parois de la capsule. Le dépôt d’énergie dans l’organisme est seulement dû aux rayons X : 20 keV en moyenne par désintégration. Dans ce domaine d’énergie, le parcours moyens des rayons X dans la matière vivante n’est que de quelques cm. Pour cette raison, la majeure partie de l’énergie déposée dans l’organisme l’est dans la prostate ou à proximité immédiate. Ceci explique que l’on puisse garder ces implants alors que dans d’autres curiethérapies les sources ne sont gardées que le temps de l’hospitalisation.
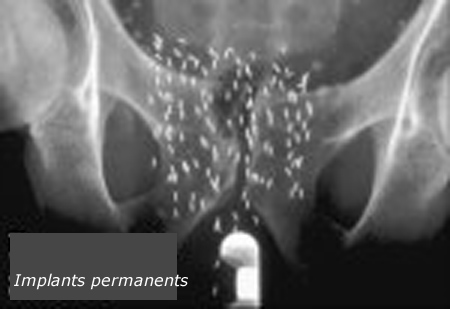
Curiethérapies de la prostate
Des sources scellées d’iode 125 (période de 60 jours) sont utilisées en curiethérapie pour les cancers de la prostate. Les sources, de quelques millimètres de long, sont mises en place de façon permanente dans la prostate du patient. Elles ont une activité unitaire comprise entre 10 et 25 MBq et un traitement nécessite environ une centaine de grains représentant une activité totale de 1500 MBq, permettant de délivrer une dose prescrite de 145 Gy à la prostate.
© Kimmel Cancer Center at Jefferson/Adam Dicker
De 40 à 130 implants sont installés dans la prostate, le nombre étant déterminé par le volume de la prostate à traiter. Ces implants restent à demeure. Cependant ils perdent complètement leur radioactivité au bout d’un temps à la fois long et court : les implants d’iode-125 au bout d’environ 6 mois, ceux de palladium-103 d’environ 3 mois.
La rapidité avec laquelle la radioactivité décroît et les atomes radioactifs se transforment en atomes non-radioactifs est déterminée par la période radioactive : 60,5 jours pour l’iode-125 et 17,7 jours pour le palladium-103. Pour délivrer aux cellules cancéreuses la même quantité de radiations, l’activité des implants au palladium est choisie au départ plus élevée qu’avec l’iode, la durée d’irradiation étant plus courte.
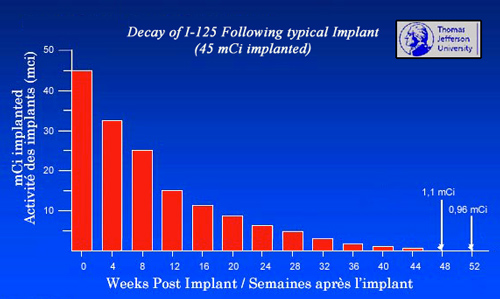
Évolution de l’activité d’implants d’iode-125
La radioactivité des implants et le nombre d’atomes radioactifs diminuent avec une rapidité déterminée par la période : 60,5 jours pour l’iode-125 et 17,7 jours pour le palladium-103. Le gros de l’activité des implants a disparu au bout de quelques périodes, 87,5 % au bout de 3 périodes, 99,9 % au bout de 10 périodes. La décroissance du palladium est 3 fois plus rapide. En six mois, il a virtuellement disparu. Le choix d’un débit de dose adapté à l’état du malade, à son âge, détermine le choix de l’un ou de l’autre.
© Kimmel Cancer Center at Jefferson/Adam.P.Dicke
La plupart des rayonnements émis par l’ode-125 et le palladium-103 ont beau être essentiellement absorbés dans la glande à traiter, un fraction touche néanmoins des structures proches comme le rectum. A cette inquiétude légitime pour le patient, s’ajoute un risque pour l’entourage tant que la radioactivité n’a pas décru suffisamment : le patient est lui-même un peu radioactif : quelques rayons gamma et X émergent aussi de son corps en raison de leur caractère pénétrant.
Le niveau de radiations émergentes après l’installation des implants reste toutefois à un niveau jugé peu dangereux pour l’entourage, mais quelques précautions permettent de réduire le risque. Il faut éviter des contacts prolongés avec des femmes enceintes ou avec de jeunes enfants (comme les prendre sur les genoux) durant les 3 ou 6 mois nécessaires pour que la radioactivité disparaisse, mais une accolade, une embrassade ou une poignée de mains sont parfaitement sures.
Les autres articles sur le sujet « Radiothérapie Avancée »
Curiethérapies
La plus ancienne thérapie nucléaire aujourd’hui modernisée La Curiethérapie est la plus anc[...]
Radiothérapies métaboliques
Des radioisotopes en interne à but thérapeutique Les applications des radioisotopes en médecine n[...]
Protonthérapies
La protonthérapie : une radiothérapie aboutie et de précision La protonthérapie consiste à traite[...]
Hadronthérapies
Autres thérapies nucléaires avancées … Les hadrons sont des particules élémentaires dont le[...]