Le radon et ses descendants
Radon dans l’environnement
La concentration du radon dans l’air dépend de la nature des sols et de nombreux facteurs météorologiques comme la pression atmosphérique, la température, l’humidité, les précipitations, la vitesse du vent. On a observé que la concentration du radon augmentait significativement après un orage. Au cours de l’année dans le Massif Central, février est le mois de la plus faible et octobre celui de la plus forte concentration .
© IRSN
Découvert en 1899, le radon est un gaz d’origine naturelle, émanant du sol, inodore, incolore, insipide. C’est un gaz rare, donc chimiquement inerte, mais soluble dans l’eau. Généralement, le radon se dilue rapidement dans l’atmosphère dès qu’il atteint la surface du sol.
Situé dans la tableau de Mendeleiev entre l’uranium et le plomb, le radon est un atome lourd. Sa densité est la plus élevée de tous les gaz. Il tend à s’accumuler dans les espaces clos comme les maisons.
Le radon migre du sol jusqu’à l’atmosphère où il est présent en quantité infime. Sa concentration varie fortement dans l’espace et dans le temps, en fonction notamment de la géologie, des conditions météorologiques. On ne lui prêterai qu’un intérêt anecdotique s’il ne constituait, du fait de son extrême radioactivité, la première cause d’irradiation parmi les sources naturelles de rayonnements. L’inhalation du radon et de ses descendants représente pour la population française le tiers de l’exposition moyenne aux rayonnements ionisants.
Le radon provient de la désintégration de l’uranium dans la croûte terrestre. De ce fait, on le trouve partout à la surface de la terre. Sa période radioactive de 3,82 jours est très courte, mais il est régénéré en tant que membre de la filiation radioactive de l’uranium-238. Bien que l’uranium soit un élément naturel rare, il est présent dans la plupart des roches et surtout dans des sous-sols granitiques et volcaniques.
La nocivité du radon – un gaz inerte – est surtout due aux désintégrations alpha de ses descendants qui ne sont ni gazeux, ni inertes … La désintégration du radon produit du polonium-218, qui se transforme ensuite successivement en plomb-214, bismuth-214 et polonium-214 pour aboutir au plomb-210. Cette série de transformations s’effectue dans un intervalle de temps, variable d’un noyau à l’autre, qui est de l’ordre de l’heure.
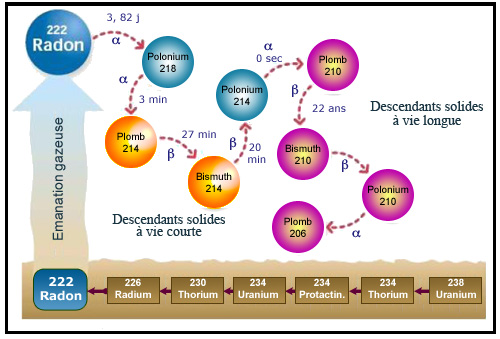
La descendance du radon
Le Radon se désintègre en donnant successivement dans un cours délai des atomes de Polonium-218, Plomb-214, Bismuth-214 et Polonium-214. Les trois premiers descendants peuvent, si inhalés, se fixer sur les poumons. Du fait de sa très courte période (16 ms), le Polonium-214 vit trop peu pour s’y fixer. Le Plomb-210, terminus de cette cascade de désintégrations, est lui-même radioactif mais sa période de 22 ans est beaucoup plus longue. De ce fait, son activité (et celle de ces descendants) représente moins de 0,5 millième de celle initiale du Radon.
© IPHC/IN2P3
Ce délai donne le temps aux trois premiers descendants (polonium-218, plomb-214, bismuth-214) de se fixer sur de microscopiques particules qui, si elles sont inhalées, se déposeront sur les cellules pulmonaires. Le descendant suivant, le polonium-214, n’a pas le temps se fixer sur les poumons par inhalation car sa durée de vie est de 1 ,6 centième de seconde.
Les émetteurs de particules alpha fixés à demeure sur les cellules pulmonaires sont dangereux. Les rayons alpha sont beaucoup plus nocifs au contact de la matière vivante que les rayons beta, car ils déposent leur énergie d’une manière très concentrée. Si on associe cette énergie aux dommages causés, le polonium-218, qui émet en propre une particule alpha de 6,0 MeV, suivie d’une seconde de 7,69 MeV quand il passe par l’étape du polonium-214, est le plus nocif de la descendance. Les trois descendants suivants, qui n’émettent que l’alpha de 7,69 MeV du polonium-214, possèdent une énergie alpha potentielle moindre.