Une variante lourde et radioactive de l’hydrogène
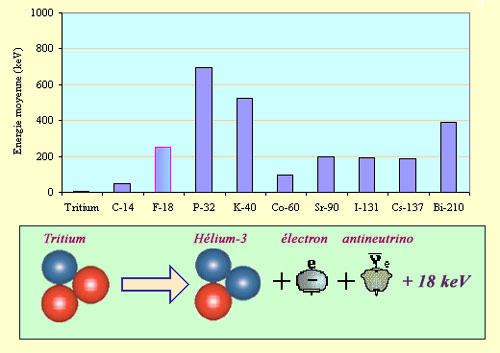
Un électron bêta de faible énergie
L’énergie emportée par l’électron du tritium est exceptionnellement faible comme le montre cette comparaison des énergies moyennes des électrons dans un certain nombre de désintégrations bêta : 5.7 keV contre plusieurs centaines de keV en général. L’énergie totale libérée, partagée entre l’électron et l’antineutrino est de 18 keV. Par ailleurs, comme la désintégration aboutit directement au noyau d’hélium dans son état normal, il n’y a pas passage par un état excité, donc pas de rayons gamma émis.
© IN2P3
Le tritium est un isotope radioactif de l’hydrogène qui émet des électrons bêta. Son noyau est constitué d’un proton et de deux neutrons. Le tritium est trois fois plus lourd que l’hydrogène ordinaire dont le noyau est réduit à un proton, et une fois et demie plus lourd que le deutérium dont le noyau est constitué d’un proton et d’un neutron.
Le tritium n’existerait pas dans notre environnement, s’il n’était produit en très petite quantité dans l’atmosphère par le rayonnement cosmique. La période radioactive de ce noyau instable est de 12,3 années, une durée de vie faible comparée à celle des déchets à vie longue des réacteurs. Cette disparition relativement rapide empêche que cet élément ait le temps de s’accumuler beaucoup.
Du fait de sa période relativement courte, le tritium est généralement considéré comme un élément très radioactif. Mais les conséquences de son caractère radioactif se trouvent heureusement atténuées du fait des caractéristiques de sa désintégration. L’énergie moyenne de l’électron est exceptionnellement faible : 5,7 keV à comparer avec plusieurs centaines de keV en général pour les désintégrations bêta. Par ailleurs, le tritium n’émet pas de rayons gamma.

Cadrans lumineux
Le tritium a remplacé le radium des peintures luminescentes pour les cadrans de montre et les instruments de bord de la navigation de nuit. Aujourd’hui, les lettres luminescentes contiennent du tritium et des substances fluorescentes qui émettent une lumière visible lorsqu’elles sont excitées par le rayonnement bêta du tritium. La fabrication, comme l’usage, ne posent aucun problème de santé. L’électron bêta ne quitte pas la peinture et le tritium n’émet pas de photon gamma.
© Musée Curie
Le tritium est très mobile comme l’hydrogène. Il se combine avec de l’oxygène pour former de l’eau tritiée. Il pénètre facilement dans l’organisme, à travers le cycle de l’eau, et entraîne une exposition interne. Toutefois le tritium s’élimine rapidement. Sa période biologique de l’ordre de 10 jours est beaucoup plus courte que les 12,3 années de sa période radioactive. Un noyau de tritium seulement sur 650 se désintègre durant un trajet dans le corps humain. En raison de la faible énergie de la désintégration, le parcours dans la matière de l’électron bêta n’excède pas quelques microns. Le tritium possède pour ces raisons une très faible radiotoxicité.
Le très court parcours des rayons bêta du tritium rend difficile la mise en évidence de sa présence. La trop faible énergie des rayons ne leur permet pas de franchir la paroi des compteurs usuels. L’hydrogène tritié est mélangé sous forme d’eau à un liquide scintillant. La quantité des scintillations observée dans le liquide mesure la quantité de tritium (youtube IRSN : la mesure du tritium).
En biologie, le tritium est utilisé pour marquer l’hydrogène et étudier son métabolisme. On a pu ainsi évaluer la durée du cycle biologique de l’hydrogène dans le corps humain entre 6 et 9 jours.
Dans la vie courante, il a remplacé le radium pour rendre luminescents les cadrans de certaines montres et les instruments de bord pour la navigation de nuit.
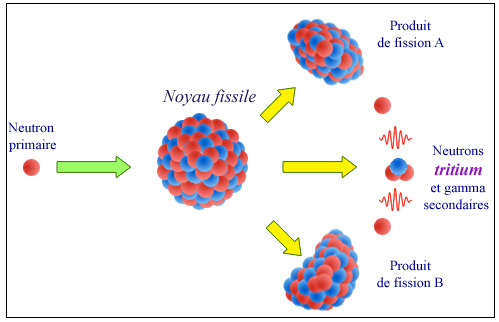
Une fission particulière…
Du tritium fait partie des effluents radioactifs issus des usines de retraitement et des installations militaires, car il est produit lors de fissions rares – des fissions ternaires – au sein du combustible des réacteurs. Un noyau de tritium remplace un des neutrons secondaires.
© IN2P3
Au sein des réacteurs, du tritium est produit par capture de neutrons dans l’eau qui sert au refroidissement, ainsi que dans le combustible nucléaire lors de fissions rares – des fissions dites ternaires. Dans le cas des réacteurs à eau pressurisée, ce tritium reste contenu dans la cuve du réacteur (les fuites sont plus importantes avec les réacteurs à eau bouillante). Ultérieurement, il se retrouve au sein de combustibles usés, dans des piscines d’entreposages puis sous forme d’effluents lors du retraitement en France de ces combustibles usés à l’usine de la Hague.
En février 2016, lors d’une opération de déchargement du combustible nucléaire, de l’eau contenant du tritium à des niveaux supérieurs à la normale s’est répandue sous la centrale d’Indian Point près de New-York. Selon la Nuclear Regularity Commission – l’autorité de sûreté américaine – cette fuite ne représenta pas de menace pour l’environnement. En effet, le tritium est particulièrement peu radiotoxique. Une fois déversée dans l’Hudson, l’eau radioactive est si diluée que le tritium devient pratiquement indétectable. Il en va de même, pour les effluents tritiés de l’usine de la Hague.
En août 2023 à Fukushima, les autorités japonaises commencèrent à rejeter dans l’océan des eaux qui avaient été contaminées et étaient stockées dans des réservoirs devenus pleins. Ces eaux avaient fait l’objet d’une décontamination poussée. Seule l’eau tritiée n’avait pu être épurée, séparée de l’eau ordinaire. Elle fut diluée. Ce rejet d’eau tritiée à Fukushima fit polémique, mais les premiers prélèvements de l’eau de mer confirmèrent un risque radioactif négligeable.
La toxicité radioactive du tritium est particulièrement faible. Ainsi, le facteur de dose de l’eau tritiée est 0,000018 millisievert par milliers de becquerels (cf. tableau de la page facteurs de doses). L’Organisation Mondiale de la Santé, l’OMS), considère que la limite d’acceptabilité d’une eau contenant du tritium est de 10 000 Becquerels par litre. Cette limite est en fait déjà basse. Il faudrait boire 2 litres d’une telle eau par jour pendant un an pour s’exposer à une dose de 0,1 mSv par an équivalente à deux semaines de radioactivité naturelle.
La limite supérieure à l’eau du robinet imposée par la règlementation française est 100 fois inférieure, de 100 Bq/litre (Cette valeur est voisine de la radioactivité émanant de notre corps humain, qui est de 100 Bq/kilogramme). Le calcul montre qu’une personne ayant bu tous les jours une eau tritiée à 100 Bq/litre s’exposerait à une dose annuelle de 0,657 µSv (millionième de sievert), qui équivaudrait environ à deux heures de radioactivité naturelle. Une clopinette … radioactive ! Très inférieure par exemple aux 4 à 30 µSv résultant d’une radio panoramique dentaire. Ces données rassurantes n’empêchèrent pas en juillet 2019 des journaux et des médias de lancer une alerte à une pollution tritium qui toucherait 6 millions de français. Alerte ou désinformation, ces buveurs d’eau du robinet exposés au maximum à 0,657 µSv purent dormir sur leurs deux oreilles !
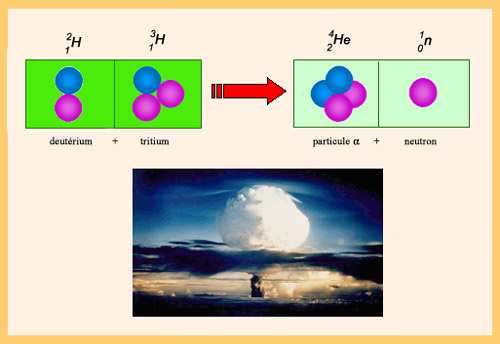
La fusion du deutérium et du tritium
La réaction de fusion du deutérium et du tritium est la réaction de fusion nucléaire qui libère le plus d’énergie : 17 MeV. Lors de la fusion, les nucléons se réorganisent pour donner une particule alpha et un neutron. C’est la formation de la particule alpha – un noyau très lié – qui est à l’origine du fort dégagement d’énergie. La réaction est recherchée dans les bombes H. Elle est utilisée au laboratoire pour produire des neutrons rapides.
© DR
La réaction de fusion du deutérium et du tritium est la réaction thermonucléaire qui libère le plus d’énergie. Cette réaction a été utilisée, notamment par les Etats-Unis et l’Union Soviétique dans les années 1950 et 1960 pour procéder à des essais de bombes thermonucléaires, ou bombes H, beaucoup plus puissantes et dévastatrices que les bombes atomiques basées sur la fission. Ces essais ont été à l’origine d’une pollution importante à proximité des pas de tirs.
Ces armes thermonucléaires nécessitent la production de quantités suffisantes de tritium. Le tritium naturel étant trop rare, ce tritium militaire est obtenu en bombardant du lithium par des neutrons. Par ailleurs, le tritium en provenance des installations militaires est à l’origine de déchets tritiés a surveiller, davantage en raison de la mobilité du tritium que de sa toxicité radioactive.
La réaction de fusion du deutérium et du tritium sera exploitée dans les réacteurs basés sur la fusion nucléaire. Il reste à prouver que de tels réacteurs pourront voir le jour. C’est l’objet des recherches entreprises à l’échelle mondiale avec le projet ITER.
Voir aussi :
Radiotoxicité potentielle
Fusion Nucléaire
Le tritium et l’environnement : Brochure de la Société Française de Radioprotection (pdf)
Le tritium : Wikipedia
Tritium or not tritium, Isabelle Jouette, Revue Générale Nucléaire (RGN) – février 2016
Tritium, Information scientifique et désinformation, Cecile Crampon, Revue Générale Nucléaire – Juillet 2019
Les autres articles sur le sujet « Principaux noyaux »
Uranium
L’uranium-235 : le seul noyau fissile existant à l’état naturel L’atome d&rsquo[...]
Plutonium-239
Plutonium-239 : un noyau fissile artificiel, redouté et recherché Quatre-vingt-quatorzième élémen[...]
Le radium
Le premier atome radioactif découvert Le radium, élément extrêmement rare, fut découvert par Pier[...]
Le carbone-14
Un radioélément produit dans l’atmosphère utilisé pour la datation Le noyau de carbone-14 c[...]
Le potassium-40
Un noyau à vie très longue et deux modes de désintégration Le potassium-40, que l’on trouve[...]
L’Iode-131
Un isotope radioactif de l’iode qui se concentre dans la thyroïde L’iode-131 est un é[...]
Césium 137
Un radio-isotope important de 30 ans de période Le césium-137 est un élément radioactif dont la d[...]
Strontium-90
Un produit de fission proche du calcium Le strontium-90 est avec le césium-137 un des principaux [...]
Technétium-99
Tous les atomes du tableau de Mendeleïev jusqu’à l’uranium sont présents dans notre e[...]